Разговор об антибактериальной терапии был бы не полным, если бы мы не поговорили о некоторых ее осложнениях, доставляющих серьезный дискомфорт как пациентам, так и медицинским работникам. Сегодня поговорим об одном из самых часто встречающихся, а именно об антибиотик-ассоциированных заболеваниях кишечника и их частном случае, исключительно нозокомиальном грозном состоянии – псевдомембранозном колите.
В классификации антибиотик-ассоциированных заболеваний кишечника как только не извращаются. Но мы собрались, чтобы понять суть, а не классификации. Поэтому предлагаю различать между собой антибиотик-ассоциированную диарею (ААД) и псевдомембранозный колит (ПМК). Первое состояние видят все, кто имеет отношение к назначению антибактериальных препаратов, второе видят исключительно в условиях стационара (ибо заболевание на 100% нозокомиальное).
Итак, антибиотик-ассоциированные диареи (ААД) в самом широком смысле слова.
Как я уже сказала, видят ее все, кто, так или иначе, назначает антибактериальные препараты. И именно это видят врачи амбулаторного звена, а никак не ПМК (исключение – онкопациенты на амбулаторной химиотерапии).
Причиной развития ААД может быть большое количество факторов:
- Макролиды, которые действуют на мотилиновые рецепторы
- Клавулановая кислота и ее метаболиты, которые стимулируют моторику тонкой кишки (в медицинском народе амокси/клавуланат давно заслужил почетное звание «большой поносогенной таблетки)
- Пенициллины, которые способны вызвать сегментарный колит
- Тетрациклины, которые напрямую бьют по слизистой ЖКТ
- Под действием самих антимикробных препаратов гибнут целые классы анаэробов, которые регулируют углеводный обмен, как результат, может начаться осмотическая диарея (и никакой это не дисбактериоз!)
- Необходимо также учитывать и сопутствующую лекарственную терапию – антациды, слабительные, препараты, содержащие лактозу и маннитол, рентген-контрасты, НПВС, антиаритмики и холиномиметики.
Поэтому в каждом случае необходимо предметно разбираться, почему именно у каждого конкретного приключилась такая побочная реакция и, если есть возможность, – понаблюдать за ним пару дней, по возможности отменив подозреваемый препарат и заменив его на что-то менее агрессивное в отношении ЖКТ.
Если пациент крайние пару месяцев находился в стационаре, где получал антибактериальную терапию, и особенно если есть данные о том, что в стационаре давно и успешно живет главный возбудитель ПМК – C. difficile – его необходимо рассматривать как возможного клиента с ПМК, ибо риск слишком велик и лечить его надо соответственно ситуации. То же самое относится к пациентам, уже имевшими эпизод ПМК в своей жизни, ибо клостридию им убили (если лечили), а вот споры ее точно остались. Я своим "клиентам" всегда говорю о необходимости предупреждать врачей в дальнейшем, что подобные состояния с ними уже случались, чтобы коллеги проявляли настороженность и не начинали с ходу колоть цефтриаксон.
Если же вы имеете дело с первым столкновением с антибиотиками, то можно понаблюдать пару дней, произведя замену препаратов (только не на бета-лактамы! я постоянно имею дело с тем, что один бета-лактам меняется на второй-третий и пациент из ААД уходит, как минимум, в антибиотик-ассоциированный колит, а то и в масштабный псевдо-мембранозный... но это о стационарных больных речь). Главное в этот период не назначать препаратов, снижающих моторику кишечника! И донести до пациента необходимость расширения питьевого режима.
А теперь поговорим о такой серьезной частности, как псевдомембранозный колит
Надо с самого начала понимать, что не всякая диарея в условиях стационара является антибиотико-ассоциированной, не каждая антибиотико-ассоциированная диарея является ПМК, но почти 100% ПМК вызвано Clostridium difficile.
Что необходимо знать об этом возбудителе.
Справочник по антибактериальной терапии медицинской школы Хопкинса сообщает следующее (автор John G. Bartlett, MD):
Clostridium difficile является спорообразующим анаэробом, продуцирующим токсины А и В, которые вызывают у людей явления колита. Причем у здоровых людей случаи колонизации не превышают 3%, а вот у госпитализированных пациентов эта цифра доходит до 20-40%.
Наибольшему риску заражения подвергаются госпитализированные пациенты или пациенты с хроническими заболеваниями, требующими медицинского ухода, лица пожилого возраста и пациенты, получающие антибактериальную терапию.
Антибиотиками-провокаторами являются:
С высоким уровнем риска: клиндамицин, цефалоспорины третьей генерации, фторхинолоны
Со средним уровнем риска: пенициллины и цефалоспорины с узким спектром, карбапенемы, макролиды, ко-тримоксазол
Низкий риск исходит от метронидазола, тетрациклинов, ванкомицина и аминогликозидов,
Вообще не отмечено риска при использовании сульфаниламидов, нитрофурантоина и фосфомицина.
Эти данные обязательно стоит учитывать, если речь идет о стационарах с высоким уровнем наличия клостридии.
В настоящее время C. difficile отдано ведущее место в возникновении нозокомальных кишечных инфекций – энтеритов, колитов, ПМК, связанных с предшествующим и, очень часто, необоснованным приемом антибиотиков. Одно время его даже посчитали «детищем антибиотиковой эры», но это не совсем так.
Основная проблема заключается в том, что мало где, даже в продвинутых странах запада, ведется регистрация заболеваний, обусловленных C. difficile, что уж говорить про нас, находящихся в условиях малой доступности микробиологической диагностики.
C. difficile, как спорообразующий микроорганизм, способен до 180 дней сохраняться в окружающей среде, с чем и связаны проблемы его распространения на предметах ухода в стационарах, а особенно в их туалетных комнатах. И тут мы снова возвращаемся к необходимости жесткого микробиологического мониторинга и соблюдения сан. эпид. режима в условиях стационаров.
Следует также помнить, что не каждая C. difficile способна вызвать ПМК. Основную роль здесь играют штаммы C. difficile, продуцирующие токсины, – энтеротоксин А и цитотоксин В, которые, высвобождаясь из микробных клеток, взаимодействуют с рецепторами на поверхности клеток кишечного эпителия, запускается механизм эндоцитоза, токсин проникает в клетку, вызывает дезорганизацию деятельности и ее гибель. Клинически это проявляется диареей, а морфологически – в виде воспаления слизистой толстой кишки и образования на ней очень характерного налета – псевдомембран
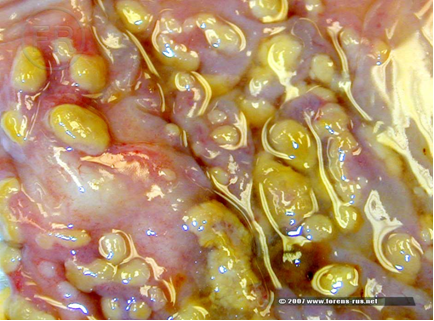
Естественно стоит упомянуть и эпидемиологические аспекты
Сразу предупреждаю – тут я окончательно потеряю скромность и буду опираться на опыт войны со зверем в условиях нашего стационара.
Как мы уже говорили, ПМК – это заболевание, носящее на 100% нозокомиальный характер, т. е. это инфекция, связанная исключительно с медицинским вмешательством. Почему? Да собственно потому, что в обычной, взрослой популяции, частота носительства C. difficile составляет не более 3%. В стационарах же этот процент подскакивает до 60%. И это всегда связано с низким уровнем сан. эпид. режима. Но не расстраивайтесь, это не наши цифры, это цифры американцев. Что творится у нас – это тайна покрытая мраком из-за недоступности микробиологической диагностики вообще и микробиологического мониторинга в частности.
Каков путь распространения?
Он стандартный – фекально-оральный. Места "гнездования" тоже понятны – туалетные комнаты и всё там находящееся.
Да, коллеги, туалетные комнаты как у пациентов, так и у персонала должны отмываться так же, как это делается в супермаркетах и отелях – то есть минимум 4 раз на день, а лучше каждые 3 часа, особенно когда в отделении бушуют антибиотиковые поносы. И делаться это должно как следует, а не как привычно. И руки всего персонала должны обрабатываться сразу по выходу из "комнаты глубокой медитации". Например, у нас в ЛПУ стараниями главной сестры на выходе из туалетных комнат на уровне глаз висят ярко красные диспенсеры с дез. средствами для обработки рук.
Вообще, по большей части, клостридию мы носим на себе, если пренебрегаем элементарной обработкой рук. И тогда клостридия расползается на спец. одежду, телефоны (которые мы же потом сами и "облизываем"), клавиатуры компьютеров, мыши, столы и т. д. и т. п. Косвенным признаком ее наличия в ординаторских, если в отделении имеются пациенты с ПМК, будет появление кишечной палки на столах, что означает, что кто-то не хочет мыть руки, выходя из туалета.
Кроме того, зверь уютно живет на матрасах и простынях в палатах, и вообще на всем, до чего дотронулся пациент-носитель, а таких носителей – каждый второй.
Из всего этого и вылезают те самые 60% носительства клостридиии в стационаре. Причем обсеменение моментальное – достаточно 3 дней.
Какие же отделения наиболее опасные по развитию ПМК – это отделения реанимации и палаты интенсивной терапии, по признаку максимального использования антибактериальных препаратов широчайшего спектра, хирургические отделения, да и, собственно, все, кто на каждый чих начинает колоть цефтриаксон (уж сколько раз твердили миру, а воз и ныне там)
Можно ли победить зверя в стационарах? Можно, если будете делать, как мы. Но это сложно, долго и надо всех уговаривать и воспитывать, прививая определенную культуру поведения (например, вбить в голову, что перчатки – не презерватив и без адекватной обработки рук толку с тех перчаток нет), и вообще надо хотеть это сделать. Во всех остальных случаях клостридия рано или поздно победит вас, как и произошло в одном стационаре нашей необъятной, которой "повезло" обзавестись клостридией, устойчивой к метронидазолу. Из разговора годичной давности я поняла, что проблема так и не решена...
Отдельно следует упомянуть взаимоотношения C. difficile и детей
С детьми картина совершенно иная. Следует запомнить, что у 30-70% ЗДОРОВЫХ новорожденных в кале присутствует C. difficile! Против 3% здоровых взрослых. При этом 90% штаммов продуцирует токсин А. И нет, это не повод немедленно начинать паниковать и бежать их санировать, так как это ЗДОРОВОЕ НОСИТЕЛЬСТВО (если, конечно, нет соответствующей клиники, которой еще никто не видел, судя по литературным источникам). В течение первого года уровень носительства снижается до 9% и далее приравнивается к взрослым 3%.
Считается, что этот "феномен" связан с несовершенством рецепторного аппарата кишечного эпителия новорожденных. Они просто не реагируют на токсин.
Что еще надо знать об эпидемиологии:
Для того, чтобы началась манифестация заболевания, помимо колонизации токсигенными штаммами клостридии (а мы уже договорились говорить о токсигенных штаммах) необходимо, чтобы пациент получил еще и лошадиную дозу антибиотиков, чаще всего цефалоспоринов третьего поколения, безусловным лидером которых является цефтриаксон. И нет, я не просто так сказала про лошадиную дозу, так как существует прямая связь между дозой и кратностью введения и развитием ААД и ПМК (а нашими препаратами, которые выигрывают на аукционах по принципу «самое дешевое хорошо», если сработают 2 грамма раз в день, но все чаще мне приходится иметь дело с 2 гр х 2 раза в день с соответствующим результатом в виде ААД... особенно когда пациент "залетный" от коллег из другого ЛПУ).
Помимо антимикробных препаратов махровые ПМК вызывает противоопухолевый метотрексат... И с этом кошмаром пациенты оказываются один на один, если они находятся на амбулаторной химиотерапии. И хорошо, если в первые часы заболевания рядом окажется понимающий ситуацию и могущий с ней справиться врач.
Кроме того, факторами развития ПМК и ААД являются тяжелые сопутствующие заболевания и возраст старше 60 лет. К слову, основную группу пациентов с ПМК как раз и составляют лица старше 60 лет, ибо носительство токсигенной клостридии в этой группе повышается в разы, если не на порядки (вот к чему приводит любовь "покапаться" в условиях стационаров).
Из интересного и пока непонятного – у лиц с ВИЧ частота ААД и ПМК такая же, как в обычной популяции, хотя, казалось бы, уж они-то точно должны были из них не вылезать. Ан нет... всё как у всех.
Уровень летальности от ПМК, к сожалению, очень высок, особенно когда заболевание не распознано и своевременно не начато лечение. Осложнениями является токсический мегаколон, который и сводит пациентов в гроб в течение первых двух суток.
На клинике останавливаться смысла нет – вся клиника указана в заголовке.
С диагностикой все плохо. Нет, все очень плохо. Во-первых, из-за полного отсутствия настороженности, во-вторых, из-за ее малодоступности и откровенной сложности. Из простого есть экспресс-тесты, но они мало у кого есть, потому что нет настороженности.
Лечение – метронидазол и ванкомицин. Схемы давно известны – это справочный материал, повторяться не буду. Единственное, что еще раз скажу – главное вовремя поставить диагноз, изолировать пациента и отмыть как палату, так и отделение до состояния зеркального блеска, иначе у вас будет уже не один, а очень много таких пациентов.
На этом позвольте закончить эту не очень приятно пахнущую, но очень необходимую тему.



