Семвелика® (Semvelica) инструкция по применению
- 📜 Инструкция по применению Семвелика®
- 💊 Состав препарата Семвелика®
- ✅ Применение препарата Семвелика®
- 📅 Условия хранения Семвелика®
- ⏳ Срок годности Семвелика®
Владелец регистрационного удостоверения:
Лекарственная форма
|
|
Семвелика® |
Раствор для подкожного введения 1.34 мг/мл (0.25/0.5/1 мг/доза): шприц-ручки 3 мл 1, 2 или 3 шт.
РУ: ЛП-008881
от 29.10.25
- Действующее
Дата переоформления: 16.12.25
|
Форма выпуска, упаковка и состав препарата Семвелика®
Раствор для п/к введения прозрачный, бесцветный или почти бесцветный.
| 1 мл | |
| семаглутид | 1.34 мг |
Вспомогательные вещества: динатрия гидрофосфата дигидрат, пропиленгликоль, фенол, хлороводородная кислота 1М раствор, натрия гидроксид 1М раствор, вода д/и.
3 мл (0.25/0.5/1 мг/доза) - картриджи, встроенные в шприц-ручки одноразовые мультидозовые для многократных инъекций (1) - пачки картонные.
3 мл (0.25/0.5/1 мг/доза) - картриджи, встроенные в шприц-ручки одноразовые мультидозовые для многократных инъекций (1) с иглами одноразовыми* (4, 6, 9, 10 или 12 шт.) - пачки картонные.
3 мл (0.25/0.5/1 мг/доза) - картриджи, встроенные в шприц-ручки одноразовые мультидозовые для многократных инъекций (2) - пачки картонные.
3 мл (0.25/0.5/1 мг/доза) - картриджи, встроенные в шприц-ручки одноразовые мультидозовые для многократных инъекций (2) с иглами одноразовыми* (8, 12 или 18 шт.) - пачки картонные.
3 мл (0.25/0.5/1 мг/доза) - картриджи, встроенные в шприц-ручки одноразовые мультидозовые для многократных инъекций (3) - пачки картонные.
3 мл (0.25/0.5/1 мг/доза) - картриджи, встроенные в шприц-ручки одноразовые мультидозовые для многократных инъекций (3) с иглами одноразовыми* (12, 18 или 27 шт.) - пачки картонные.
* Иглы одноразовые установлены в держатель картонный для игл (или без картонного держателя).
Шприц-ручка совместима с любыми иглами для шприц-ручек.
Фармакологическое действие
Семаглутид является агонистом рецепторов ГПП-1 (ГПП-1Р), произведенным методом биотехнологии рекомбинантной дезоксирибонуклеиновой кислоты (ДНК) с использованием штамма Escherichia coli с последующей модификацией и очисткой. Семаглутид представляет собой аналог ГПП-1, имеющий 94% гомологичности с человеческим ГПП-1. Семаглутид действует как агонист ГПП-1Р, который селективно связывается и активирует эти рецепторы. ГПП-1Р служат мишенями для нативного ГПП-1.
ГПП-1 является физиологическим гормоном, оказывающим сразу несколько эффектов на регуляцию концентрации глюкозы и аппетит, а также на сердечно-сосудистую систему. Влияние на концентрацию глюкозы и аппетит специфически опосредовано ГПП-1Р, расположенными в поджелудочной железе и головном мозге. Фармакологические концентрации семаглутида снижают концентрацию глюкозы крови и массу тела посредством сочетания эффектов, описанных ниже. ГПП-1Р представлены также в специфических областях сердца, сосудов, иммунной системы и почек, где их активация может оказывать сердечно-сосудистые и микроциркуляторные эффекты.
В отличие от нативного ГПП-1, продленный Т1/2 семаглутида (около 1 недели) позволяет применять его подкожно 1 раз в неделю. Связывание с альбумином является основным механизмом длительного действия семаглутида, что приводит к снижению выведения его почками и защищает от метаболического распада. Кроме того, семаглутид стабилен в отношении расщепления ферментом дипептидилпептидазой-4.
Семаглутид снижает концентрацию глюкозы крови посредством глюкозозависимой стимуляции секреции инсулина и подавления секреции глюкагона. Таким образом, при повышении концентрации глюкозы крови происходит стимуляция секреции инсулина и подавление секреции глюкагона. Механизм снижения уровня глюкозы включает также небольшую задержку опорожнения желудка в ранней постпрандиальной фазе. Во время гипогликемии семаглутид уменьшает секрецию инсулина и не снижает секреции глюкагона.
Семаглутид снижает общую массу тела и массу жировой ткани, уменьшая потребление энергии. Данный механизм затрагивает общее снижение аппетита, включая усиление сигналов насыщения и ослабление сигналов голода, а также улучшение контроля потребления пищи и снижение тяги к пище. Снижается также инсулинорезистентность, возможно за счет уменьшения массы тела. Помимо этого, семаглутид снижает предпочтение к приему пищи с высоким содержанием жиров. В исследованиях на животных было показано, что семаглутид поглощается специфическими областями головного мозга, усиливает ключевые сигналы насыщения и ослабляет ключевые сигналы голода. Воздействуя на изолированные участки тканей головного мозга, семаглутид активирует нейроны, связанные с чувством сытости, и подавляет нейроны, связанные с чувством голода.
В клинических исследованиях (КИ) семаглутид оказывал положительное влияние на липиды плазмы крови, снижал систолическое АД и уменьшал воспаление.
В исследованиях на животных семаглутид подавлял развитие атеросклероза, предупреждая дальнейшее развитие аортальных бляшек и уменьшая воспаление в бляшках.
Фармакодинамика
Все фармакодинамические исследования были проведены после 12 недель терапии (включая период увеличения дозы) в равновесной концентрации семаглутида 1 мг 1 раз в неделю.
Уровень гликемии натощак и постпрандиальный уровень гликемии
Семаглутид снижает концентрацию глюкозы натощак и концентрацию постпрандиальной глюкозы. По сравнению с плацебо терапия семаглутидом 1 мг у пациентов с сахарным диабетом 2 типа (СД2) приводила к снижению концентрации глюкозы с точки зрения абсолютного изменения от исходного значения (ммоль/л) и относительного снижения по сравнению с плацебо (%) в отношении: концентрации глюкозы натощак (1.6 ммоль/л; 22%); концентрации глюкозы через 2 ч после приема пищи (4.1 ммоль/л; 37%); средней суточной концентрации глюкозы (1.7 ммоль/л; 22%) и постпрандиальных пиков концентрации глюкозы за 3 приема пищи (0.6-1.1 ммоль/л). Семаглутид снижал концентрацию глюкозы натощак после введения первой дозы.
Функция β-клеток поджелудочной железы и секреция инсулина
Семаглутид улучшает функцию β-клеток поджелудочной железы. После в/в струйного введения глюкозы пациентам с СД2 семаглутид по сравнению с плацебо улучшал 1-ю и 2-ю фазы инсулинового ответа с 3-кратным и 2-кратным повышением, соответственно, и увеличивал максимальную секреторную активность β-клеток поджелудочной железы после теста стимуляции аргинином. Кроме того, по сравнению с плацебо терапия семаглутидом увеличивает концентрации инсулина натощак.
Секреция глюкагона
Семаглутид снижает концентрацию глюкагона натощак и постпрандиальную концентрацию глюкагона. У пациентов с СД2 семаглутид приводит к относительному снижению концентрации глюкагона по сравнению с плацебо: концентрации глюкагона натощак (8–21%), постпрандиального глюкагонового ответа (14–15%) и средней суточной концентрации глюкагона (12%).
Глюкозозависимая секреция инсулина и глюкозозависимая секреция глюкагона
Семаглутид снижал высокую концентрацию глюкозы в крови, стимулируя секрецию инсулина и снижая секрецию глюкагона глюкозозависимым способом. Скорость секреции инсулина после введения семаглутида пациентам с СД2 была сопоставима с таковой у здоровых добровольцев.
Во время индуцированной гипогликемии семаглутид по сравнению с плацебо не изменял контррегуляторный ответ повышения концентрации глюкагона, а также не усугублял снижение концентрации С-пептида у пациентов с СД2.
Опорожнение желудка
Семаглутид вызывал небольшую задержку раннего постпрандиального опорожнения желудка, тем самым снижая скорость поступления постпрандиальной глюкозы в кровь.
Масса тела и состав тела
Наблюдалось большее снижение массы тела при применении семаглутида по сравнению с изученными препаратами сравнения (плацебо, ситаглиптином, эксенатидом замедленного высвобождения (ЗB), дулаглутидом и инсулином гларгин) (см. подраздел "Клиническая эффективность и безопасность"). Потеря массы тела при применении семаглутида происходила преимущественно за счет потери жировой ткани, превышающей потерю мышечной массы в 3 раза.
Аппетит, потребление калорий и выбор продуктов питания
По сравнению с плацебо семаглутид снизил потребление калорий на 18–35% во время трех последовательных приемов пищи аd libitum. Этому способствовали стимулированные семаглутидом подавление аппетита как натощак, так и после приема пищи, улучшенный контроль потребления пищи, ослабление тяги к еде, особенно с высоким содержанием жиров.
Липиды натощак и постпрандиальные липиды
По сравнению с плацебо семаглутид снижал концентрации триглицеридов и холестерина липопротеинов очень низкой плотности (ЛПОНП) натощак на 12 и 21% соответственно. Постпрандиальное увеличение концентрации триглицеридов и холестерина ЛПОНП в ответ на прием пищи с высоким содержанием жиров снизилось более чем на 40%.
Электрофизиология сердца (ЭФс)
Влияние семаглутида на процесс реполяризации в сердце было протестировано в исследовании ЭФс. Применение семаглутида в дозах, превышающих терапевтические (в равновесной концентрации до 1.5 мг), не приводило к удлинению скорректированного интервала QТ.
Клиническая эффективность и безопасность
Как улучшение гликемического контроля, так и снижение сердечно-сосудистой заболеваемости и смертности являются неотъемлемой частью лечения СД2.
Эффективность и безопасность семаглутида в дозах 0.5 мг и 1 мг оценивались в 6 рандомизированных контролируемых КИ фазы 3а. Из них 5 КИ в качестве основной цели оценивали эффективность гликемического контроля, в то время как 1 КИ оценивало в качестве основной цели сердечно-сосудистый исход. В дополнение были проведены 2 КИ семаглутида фазы 3 с участием японских пациентов.
В дополнение было проведено исследование фазы 3b для сравнения эффективности и безопасности семаглутида в дозах 0.5 мг и 1 мг 1 раз в неделю с дулаглутидом в дозах 0.75 мг и 1.5 мг 1 раз в неделю соответственно. Также было проведено КИ фазы 3b с целью изучения эффективности и безопасности семаглутида в качестве дополнения к лечению ингибитором натрий-зависимого переносчика глюкозы 2-го типа (SGLT2).
Терапия семаглутидом продемонстрировала устойчивое, статистически превосходящее и клинически значимое улучшение показателя гликированного гемоглобина (HbA1c) и снижение массы тела на срок до 2 лет по сравнению с плацебо и лечением с активным контролем (ситаглиптином, инсулином гларгин, эксенатидом ЗB и дулаглутидом).
Возраст, пол, раса, этническая принадлежность, исходные значения ИМТ и массы тела (кг), длительность сахарного диабета и почечная недостаточность не повлияли на эффективность семаглутида.
Кроме того, было проведено КИ фазы 3b с целью изучения действия/влияния семаглутида по сравнению с инсулином аспарт, оба в качестве дополнения к метформину и оптимизированной терапии инсулином гларгин 100 ЕД.
Монотерапия
Монотерапия семаглутидом в дозах 0.5 мг и 1 мг 1 раз в неделю в течение 30 недель по сравнению с плацебо привела к статистически более значимому снижению показателей HbA1c (-1.5% и -1.6% против 0 %, соответственно), глюкозы плазмы натощак (ГПН) (-2.5 ммоль/л и -2.3 ммоль/л, против -0.6 ммоль/л соответственно) и массы тела (-3.7 кг и -4.5 кг против -1.0 кг, соответственно).
Семаглутид по сравнению с ситаглиптином, оба в комбинации с 1–2 пероральными гипогликемическими препаратами (ПГГП) (метформином и/или препаратами группы тиазолидиндиона)
Терапия семаглутидом 0.5 мг и 1 мг 1 раз в неделю в течение 56 недель по сравнению с ситаглиптином привела к устойчивому и статистически более значимому снижению показателей HbA1c (-1.3% и -1.6% против -0.5%, соответственно), ГПН (-2.1 ммоль/л и -2.6 ммоль/л против -1.1 ммоль/л, соответственно) и массы тела (-4.3 кг и -6.1 кг против -1.9 кг, соответственно).
Терапия семаглутидом 0.5 мг и 1 мг по сравнению с ситаглиптином значительно снижала систолическое АД от исходного значения в 132.6 мм рт.ст. (-5.1 мм рт.ст. и -5.6 мм рт.ст. против -2.3 мм рт.ст., соответственно). Изменений диастолического АД не происходило.
Семаглутид по сравнению с дулаглутидом, оба в комбинации с метформином
Терапия семаглутидом 0.5 мг по сравнению с дулаглутидом 0.75 мг, оба 1 раз в неделю на протяжении 40 недель, привела к устойчивому и статистически превосходящему снижению показателей HbA1c (-1.5% против -1.1%), ГПН (-2.2 ммоль/л против -1.9 ммоль/л) и массы тела (-4.6 кг против -2.3 кг), соответственно.
Терапия семаглутидом 1 мг по сравнению с дулаглутидом 1.5 мг (оба 1 раз в неделю на протяжении 40 недель) привела к устойчивому и статистически превосходящему снижению показателей HbA1c (-1.8% против -1.4%), ГПН (-2.8 ммоль/л против -2.2 ммоль/л) и массы тела (-6.5 кг против -3.0 кг) соответственно.
Семаглутид по сравнению с эксенатидом ЗB, оба в комбинации с метформином или метформином совместно с производным сульфонилмочевины
Терапия семаглутидом 1 мг 1 раз в неделю на протяжении 56 недель по сравнению с эксенатидом ЗB 2.0 мг привела к устойчивому и статистически более значимому снижению показателей HbA1c (-1.5% против -0.9%), ГПН (-2.8 ммоль/л против -2.0 ммоль/л) и массы тела (-5.6 кг против -1.9 кг), соответственно.
Семаглутид по сравнению с инсулином гларгин, оба в комбинации с 1–2 ПГГП (монотерапия метформином или метформин с производным сульфонилмочевины)
Терапия препаратом семаглутид в дозах 0.5 и 1 мг 1 раз в неделю по сравнению с инсулином гларгин в течение 30 недель привела к статистически более значимому снижению показателей HbA1c (-1.2 и -1.6% против -0.8% соответственно) и массы тела (-3.5 кг и -5.2 кг против +1.2 кг, соответственно).
Снижение показателя ГПН было статистически более значимым для семаглутида 1 мг по сравнению с инсулином гларгин (-2.7 ммоль/л против -2.1 ммоль/л). Не наблюдалось статистически более значимого снижения показателя ГПН для семаглутида 0.5 мг (-2.0 ммоль/л против -2.1 ммоль/л).
Доля пациентов, у которых наблюдались тяжелые или подтвержденные (<3.1 ммоль/л) эпизоды гипогликемии, была ниже при применении семаглутида 0.5 мг (4.4%) и семаглутида 1 мг (5.6%) по сравнению с инсулином гларгин (10.6%).
Больше пациентов достигли показателя HbA1c <7% без тяжелых или подтвержденных эпизодов гипогликемии и без набора веса при применении семаглутида 0.5 мг (47%) и 1 мг (64%) по сравнению с инсулином гларгин (16%).
Семаглутид по сравнению с плацебо, оба в комбинации с базальным инсулином
Терапия семаглутидом в дозах 0.5 и 1 мг по сравнению с плацебо в течение 30 недель привела к статистически более значимому снижению показателей HbA1c (-1.4% и -1.8% против -0.1%, соответственно), ГПН (-1.6 и -2.4 ммоль/л против -0.5 ммоль/л, соответственно) и массы тела (-3.7 кг и -6.4 кг против -1.4 кг, соответственно). Частота тяжелых или подтвержденных эпизодов гипогликемии существенно не различалась при применении препарата семаглутид и плацебо. Доля пациентов с показателем HbA1c<8% на скрининге, сообщивших о тяжелых или подтвержденных (<3.1 ммоль/л) эпизодах гипогликемии, была выше при применении препарата семаглутид по сравнению с плацебо и сопоставима с долей пациентов с показателем HbA1c> 8% на скрининге.
Семаглутид по сравнению с плацебо в качестве дополнения к терапии ингибитором SGLT2 (в качестве монотерапии или в комбинации с производными сульфонилмочевины или метформином)
Терапия семаглутидом в дозе 1 мг 1 раз в неделю в качестве дополнения к терапии ингибитором SGLT2 (в качестве монотерапии или в комбинации с производными сульфонилмочевины или метформином) по сравнению с плацебо раз в неделю в течение 30 недель привела к статистически значимому снижению показателей HbA1c (-1.5% против -0.1% соответственно), ГПН (-2.2 ммоль/л против 0 ммоль/л соответственно) и массы тела (-4.7 кг против -0.9 кг соответственно).
Семаглутид по сравнению с инсулином аспарт в качестве дополнения к терапии инсулином гларгин в комбинации с метформином
В 52-недельное открытое КИ было рандомизировано 1748 пациентов в соотношении 1:1 с неадекватно контролируемым СД2 после 12-недельного подготовительного периода на терапии инсулином гларгин и метформином для применения семаглутида (0.5 мг, либо 1.0 мг) 1 раз в неделю или инсулина аспарт 3 раза/сут. Включенная популяция имела среднюю продолжительность диабета 13.4 года и средний показатель HbA1c 6.5–7.5%.
На 52-й неделе показатель HbA1c снизился на 1.5% при применении семаглутида и на 1.2% на терапии инсулином аспарт.
Количество эпизодов тяжелых гипогликемий в обеих группах терапии было низким (4 эпизода при применении семаглутида и 7 эпизодов на терапии инсулином аспарт).
Средняя исходная масса тела снизилась на 4.1 кг при применении семаглутида и увеличилась на 2.8 кг на терапии инсулином аспарт, а расчетная разница в лечении составила –6.99 кг (95% ДИ от –7.41 до –6.57) на 52-й неделе.
Комбинация с монотерапией производным сульфонилмочевины
На 30-й неделе КИ (см. подраздел "Оценка влияния на сердечно-сосудистую систему") была произведена оценка подгруппы из 123 пациентов, находящихся на монотерапии производным сульфонилмочевины. На 30-й неделе показатель HbA1c снизился на 1.6% и 1.5% при применении препарата семаглутид в дозах 0.5 и 1 мг соответственно и увеличился на 0.1% при применении плацебо.
Комбинация с предварительно смешанным инсулином ± 1–2 ПГГП
На 30-й неделе КИ (см. подраздел "Оценка влияния на сердечно-сосудистую систему") была произведена оценка подгруппы из 867 пациентов‚ находящихся на терапии предварительно смешанным инсулином (в комбинации или без 2 ПГГП). На 30-й неделе показатель HbA1c снизился на 1.3% и 1.8% при применении препарата семаглутид в дозах 0.5 и 1 мг, соответственно, и снизился на 0.4 % при применении плацебо.
Соотношение пациентов, достигших целевого снижения показателя HbA1c
До 79% пациентов достигли целей лечения в отношении снижения показателя HbA1c <7% и доля таких пациентов была значительно больше при применении семаглутида по сравнению с пациентами, получавшими ситаглиптин, эксенатид 3B, инсулин гларгин, дулаглутид и плацебо.
Доля пациентов, достигших показателя HbA1c менее 7% без тяжелых или подтвержденных эпизодов гипогликемии и без набора веса, была значительно больше при применении семаглутида в дозах 0.5 и 1 мг (до 66% и 74%, соответственно) по сравнению с пациентами, получавшими ситаглиптин (27%), эксенатид 3B (29%), инсулин гларгин (16%), дулаглутид 0.75 мг (44%) и дулаглутид 1.5 мг (58%).
Масса тела
Монотерапия семаглутидом 1 мг или терапия в комбинации с 1–2 лекарственными препаратами приводила к статистически большему снижению массы тела (потеря составляла до 6.5 кг) по сравнению с терапией плацебо, ситаглиптином, эксенатидом 3B, инсулином гларгин или дулаглутидом. Снижение массы тела было устойчивым на срок до 2 лет.
После одного года терапии потери массы ≥5% и ≥10% достигло большее количество пациентов, получавших семаглутид 0.5 мг (46% и 13%) и 1 мг (10%, 62% и 24%), по сравнению с пациентами, находившимися на терапии активными препаратами сравнения ситаглиптином и эксенатидом 3B (до 18% и до 4%).
В КИ длительностью 40 недель потери массы ≥5% и ≥10% достигло большее количество пациентов, получавших препарат семаглутид 0.5 мг (44% и 14%), по сравнению с пациентами, получавшими дулаглутид 0.75 мг (23% и 3%). Потери массы ≥5% и ≥10% достигло большее количество пациентов, получавших семаглутид 1 мг (до 63% и 27%), по сравнению с пациентами, получавшими дулаглутид 1.5 мг (30% и 8%).
В сердечно-сосудистом КИ потери массы тела ≥5% и ≥10% достигло большее количество пациентов, получавших семаглутид 0.5 мг (36% и 13%) и 1 мг (47% и 20%), по сравнению с пациентами, получавшими плацебо 0.5 мг (18% и 6%) и 1 мг (19% и 7%).
ГПН и постпрандиальное увеличение концентрации глюкозы
Во время всех трех ежедневных приемов пищи семаглутид 0.5 мг и 1 мг показал значительное снижение концентрации ГПН до 2.8 ммоль/л и снижение постпрандиального прироста концентрации глюкозы до 1.2 ммоль/л (разница между значениями до и после еды, полученная после трех приемов пищи) (в дополнение см. подраздел "Фармакодинамика").
Функция β-клеток поджелудочной железы и инсулинорезистентность
В ходе терапии семаглутидом 0.5 мг и 1 мг произошло улучшение функции β-клеток поджелудочной железы и уменьшение инсулинорезистентности, что подтверждается оценкой гомеостатических моделей функции β-клеток поджелудочной железы (НОМА-В) и инсулинорезистентности (HOMA-IR) (в дополнение см. подраздел "Фармакодинамика").
Липиды
Во время КИ семаглутида наблюдалось улучшение профиля липидов крови натощак, преимущественно в группе, получавшей дозу 1 мг (в дополнение см. подраздел "Фармакодинамика").
Оценка влияния на сердечно-сосудистую систему
3297 пациентов с СД2 и высоким СС риском были рандомизированы в двойное слепое КИ длительностью 104 недели на получение семаглутида 0.5 мг или 1 мг 1 раз в неделю либо плацебо 0.5 мг или 1 мг в дополнение к стандартной терапии сердечно-сосудистых заболеваний в течение последующих двух лет.
Терапия семаглутидом привела к снижению на 26% риска первичного комбинированного исхода, включающего смерть по причине сердечно-сосудистой патологии, инфаркт миокарда (ИМ) без смертельного исхода и инсульт без смертельного исхода. В первую очередь это было обусловлено значительным уменьшением частоты инсульта без смертельного исхода (39%) и незначительным уменьшением частоты ИМ без смертельного исхода (26%), но без изменений в частоте смерти по причине сердечно-сосудистой патологии.
Значительно снизился риск реваскуляризации миокарда или периферических артерий, в то время как риск нестабильной стенокардии, требующей госпитализации, и риск госпитализации по причине сердечной недостаточности снизились незначительно.
Микроциркуляторные исходы включали в себя 158 новых или ухудшившихся случаев нефропатии. Относительный риск в отношении времени до возникновения нефропатии (новые случаи развития персистирующей макроальбуминурии, персистирующее удвоение сывороточной концентрации креатинина, необходимость в постоянной заместительной почечной терапии и смерть по причине болезни почек) составил 0.64.
В дополнение к стандартной терапии сердечно-сосудистых заболеваний терапия семаглутидом в дозах 0.5 мг и 1 мг по сравнению с плацебо 0.5 мг и 1 мг в течение 104 недель привела к значительному и устойчивому снижению от исходных значений показателя HbA1c (-1.1% и -1.4% против -0.4% и -0.4 %, соответственно).
Артериальное давление
Наблюдалось значительное снижение среднего систолического АД при применении семаглутида 0.5 мг (3.5–5.1 мм рт.ст.) и 1 мг (5.4-7.3 мм рт.ст.) в комбинации с ПГГП или базальным инсулином. Не отмечалось значительной разницы по показателям диастолического АД между семаглутидом и препаратами сравнения.
Доклинические данные по безопасности
По доклиническим данным, полученных в исследованиях фармакологической безопасности, токсичности повторных доз и генотоксичности, не выявлено какой-либо опасности для человека. В двухлетних исследованиях канцерогенности у крыс и мышей при клинически значимых концентрациях семаглутид стал причиной развития опухолей С-клеток щитовидной железы без смертельного исхода. Опухоли C-клеток щитовидной железы без смертельного исхода, наблюдаемые у крыс, характерны для группы аналогов ГПП-1. Считается, что в отношении людей данный риск является низким, но не может быть полностью исключен.
Фармакокинетика
Препарат подходит для введения 1 раз в неделю, т.к. Т1/2 семаглутида равен приблизительно 1 неделе.
Всасывание
Время достижения Сmax в плазме составило от 1 до 3 дней после введения дозы препарата.
Равновесная концентрация препарата (AUC0-24) достигалась спустя 4–5 недель однократного еженедельного применения препарата. После п/к введения семаглутида в дозах 0.5 мг и 1 мг средние показатели его равновесной концентрации у пациентов c СД2 составили около 16 нмоль/л и 30 нмоль/л соответственно.
Экспозиция для доз семаглутида 0.5 мг и 1 мг увеличивается пропорционально введенной дозе. При п/к введении семаглутида в переднюю брюшную стенку, бедро или плечо достигается сходная экспозиция.
Абсолютная биодоступность семаглутида после п/к введения составила 89%.
Распределение
Средний Vd семаглутида в тканях после п/к введения пациентам с СД2 составил приблизительно 12.5 л. Семаглутид в значительной степени связывался с альбумином плазмы крови (>99%).
Метаболизм
Семаглутид метаболизируется посредством протеолитического расщепления пептидной основы белка и последующего β-окисления жирной кислоты боковой цепи.
Выведение
ЖКТ и почки являются основными путями выведения семаглутида и его метаболитов. 2/3 введенной дозы семаглутида выводится почками, 1/3 - через кишечник.
Приблизительно 3% от введенной дозы выводится почками в виде неизмененного семаглутида.
У пациентов с СД2 клиренс семаглутида составил около 0.05 л/ч. С элиминационным Т1/2, равным примерно 1 неделе, семаглутид будет присутствовать в общем кровотоке в течение примерно 5 недель после введения последней дозы препарата.
Фармакокинетика у особых групп пациентов
Не требуется коррекции дозы семаглутида в зависимости от возраста, пола, расовой и этнической принадлежности, массы тела, наличия почечной или печеночной недостаточности.
Возраст. На основании данных, полученных в ходе КИ фазы 3а, включавших пациентов в возрасте от 20 до 86 лет, показано, что возраст не влиял на фармакокинетику семаглутида.
Пол. Пол не влиял на фармакокинетику семаглутида.
Раса. Расовая группа (европеоидная, негроидная, монголоидная) не влияла на фармакокинетику семаглутида.
Этническая принадлежность. Этническая принадлежность (латиноамериканская) не влияла на фармакокинетику семаглутида.
Масса тела. Масса тела влияла на экспозицию семаглутида. Более высокая масса тела приводит к более низкой экспозиции. Дозы семаглутида, равные 0.5 мг и 1 мг, обеспечивают достаточную экспозицию препарата в диапазоне массы тела от 40 кг до 198 кг.
Почечная недостаточность. Показано, что почечная недостаточность не оказывала клинически значимого эффекта на фармакокинетику семаглутида у пациентов с различной степенью почечной недостаточности (легкой, средней, тяжелой или у пациентов, находящихся на диализе) по сравнению с пациентами с нормальной функцией почек в исследовании с применением однократной дозы семаглутида, равной 0.5 мг. Сходные результаты были получены в КИ фазы 3а для пациентов с СД2 и почечной недостаточностью, хотя опыт применения у пациентов с терминальной стадией заболевания почек был ограничен.
Печеночная недостаточность. Печеночная недостаточность не влияла на экспозицию семаглутида. Фармакокинетические свойства семаглутида оценивались в ходе исследования однократной дозы семаглутида, равной 0.5 мг, у пациентов с различной степенью печеночной недостаточности (легкой, средней, тяжелой) по сравнению с пациентами с нормальной функцией печени.
Дети и подростки
Исследований семаглутида у детей и подростков до 18 лет не проводили.
Показания препарата Семвелика®
Препарат Семвелика® показан к применению у взрослых пациентов с СД2 на фоне диеты и физических упражнений для улучшения гликемического контроля в качестве:
- монотерапии;
- комбинированной терапии с другими ПГГП - метформином, метформином и производным сульфонилмочевины, метформином и/или тиазолидиндионом - у пациентов, не достигших адекватного гликемического контроля при проведении предшествующей терапии;
- комбинированной терапии с инсулином у пациентов, не достигших адекватного гликемического контроля на терапии семаглутидом и метформином.
Препарат Семвелика® показан для снижения риска развития больших сердечно-сосудистых событий* у пациентов с СД2 и высоким сердечно-сосудистым риском в качестве дополнения к стандартному лечению сердечно-сосудистых заболеваний (на основании анализа времени наступления первого большого сердечно-сосудистого события - см. раздел "Фармакологическое действие", подраздел "Оценка влияния на сердечно-сосудистую систему").
* Большие сердечно-сосудистые события включают: смерть по причине сердечно-сосудистой патологии, ИМ без смертельного исхода, инсульт без смертельного исхода.
| Код МКБ-10 | Показание |
| E11 | Сахарный диабет 2 типа |
Режим дозирования
Начальная доза препарата Семвелика® составляет 0.25 мг 1 раз в неделю. После 4 недель применения дозу следует увеличить до 0.5 мг 1 раз в неделю. Для дальнейшего улучшения гликемического контроля после как минимум 4 недель применения препарата в дозе 0.5 мг 1 раз в неделю, дозу можно увеличить до 1 мг 1 раз в неделю.
Доза препарата Семвелика® 0.25 мг не является терапевтической. Не рекомендуется введение более 1 мг в неделю.
Схема терапии препаратом Семвелика® представлена ниже в таблице 1.
Таблица 1. Схема увеличения дозы препарата Семвелика®
| Неделя терапии | Доза в неделю/Одна инъекция |
| Неделя 1-4 (начальная доза) | 0.25 мг |
| Неделя 5-8 | 0.5 мг |
| Поддерживающая (терапевтическая) доза Неделя 9 и далее | 1 мг |
Препарат Семвелика® может применяться в виде монотерапии или в комбинации с одним гипогликемическим препаратом или более (см. подраздел "Клиническая эффективность и безопасность").
При добавлении препарата Семвелика® к предшествующей терапии метформином и/или тиазолидиндионом либо ингибитором SGLT2 терапию метформином и/или тиазолидиндионом либо ингибитором SGLT2 можно продолжить в прежних дозах.
При добавлении препарата Семвелика® к проводимой терапии производным сульфонилмочевины или инсулином следует предусмотреть снижение дозы производного сульфонилмочевины или инсулина с целью снижения риска возникновения гипогликемий (см. раздел "Особые указания"). Применение препарата Семвелика® не требует проведения самоконтроля концентрации глюкозы крови. Самостоятельный мониторинг концентрации глюкозы в крови необходим для коррекции дозы сульфонилмочевины и инсулина, особенно в начале лечения препаратом Семвелика® и при снижении дозы инсулина. Рекомендуется использовать поэтапный подход к снижению дозы инсулина.
Пропуск дозы
В случае пропуска дозы препарат Семвелика® следует ввести как можно быстрее в течение 5 дней с момента запланированного введения дозы. Если продолжительность пропуска составляет более 5 дней, пропущенную дозу не нужно вводить. Следующую дозу препарата Семвелика® следует ввести в обычный (запланированный) день. В каждом случае пациенты могут возобновить их обычный однократный еженедельный график введения.
Особые клинические группы пациентов
Пациенты пожилого возраста (>65 лет)
Не требуется коррекции дозы в зависимости от возраста. Опыт применения семаглутида у пациентов в возрасте 75 лет и старше ограничен.
Пациенты с печеночной недостаточностью
Не требуется коррекции дозы у пациентов с печеночной недостаточностью (см. раздел "Фармакокинетика"). Опыт применения семаглутида у пациентов с печеночной недостаточностью тяжелой степени ограничен; применение препарата Семвелика® у таких пациентов противопоказано.
Пациенты с почечной недостаточностью
Не требуется коррекции дозы у пациентов с почечной недостаточностью. Опыт применения препарата у пациентов с терминальной стадией почечной недостаточности отсутствует; применение препарата Семвелика® у таких пациентов противопоказано.
Дети и подростки
Применение препарата Семвелика® у детей и подростков в возрасте до 18 лет противопоказано в связи с отсутствием данных по безопасности и эффективности.
Способ применения
Препарат Семвелика® применяют 1 раз в неделю в любое время, независимо от приема пищи.
Препарат Семвелика® вводят подкожно (п/к) в живот, бедро или плечо. Место инъекции может изменяться без коррекции дозы. Препарат Семвелика® нельзя вводить в/в и в/м.
При необходимости день еженедельного введения можно менять при условии, что интервал времени между двумя инъекциями составляет не менее 3 дней (>72 ч). После нового дня введения следует продолжить введение препарата 1 раз неделю.
Руководство по использованию предварительно заполненной шприц-ручки для препарата Семвелика®
Внимательно прочтите данную инструкцию перед применением предварительно заполненной шприц-ручки с препаратом Семвелика®.
Семвелика® (0.25/0.5/1 мг/доза) - раствор для п/к введения в предварительно заполненной шприц-ручке, которая позволяет вводить дозы 0.25, 0.5 и 1 мг. Шприц-ручка предназначена для титрации дозы 0.25 мг и поддержания терапевтических доз 0.5 и 1 мг. Одна шприц-ручка содержит 3 мл раствора.
Варианты использования шприц-ручки при введении препарата Семвелика®:
1. Титрация дозы:
- 4 инъекции по 0.25 мг;
- 4 инъекции по 0.5 мг;
- 1 инъекция по 1 мг.
2. Поддержание терапевтической дозы:
- 4 инъекции по 1 мг.
Шприц-ручка предназначена для использования с одноразовыми инъекционными иглами длиной до 8 мм. В упаковку препарата Семвелика® включены иглы. Шприц-ручка совместима с любыми иглами для шприц-ручек. Иглы могут не входить в комплект с препаратом.
Перед каждой инъекцией необходимо использовать новую иглу. После инъекции хранить и транспортировать шприц-ручку необходимо без иглы. Это предотвращает непроходимость игл, загрязнение, заражение, вытекание раствора и введение некорректной дозы препарата.
Утилизировать иглы необходимо согласно местным требованиям, соблюдая нормы и правила обращения с потенциально инфицированными материалами.
Шприц-ручка должна использоваться только одним человеком и не должна передаваться третьим лицам.
Если препарат Семвелика® в шприц-ручке выглядит иначе, чем бесцветный прозрачный раствор, то применять его нельзя.
Не следует подвергать шприц-ручку воздействию низких (ниже 2°С) и высоких (выше 30°С) температур. Не следует помещать ее в морозильную камеру. Шприц-ручку нельзя замораживать.
Использованная шприц-ручка подлежит утилизации и не должна повторно эксплуатироваться (нельзя повторно заполнять шприц-ручку).
Транспортировать шприц-ручку при высоких/низких температурах воздуха лучше в специальном термопенале или термосумке.
Храните шприц-ручку и иглы в недоступном месте.
Не следует пытаться самостоятельно ремонтировать шприц-ручку или разбирать ее на части.
Необходимо проконсультироваться с лечащим врачом (специалистом) по поводу применения шприц-ручки. Попросите продемонстрировать правильное использование шприц-ручки. Первая инъекция препарата должна проводиться под контролем врача или медсестры.
Внимательно прочитайте этикетку на шприц-ручке и убедитесь в том, что это именно тот лекарственный препарат, который Вам назначил врач, и в нужной Вам дозировке, а также проверьте срок годности препарата. Затем посмотрите на представленные ниже иллюстрации, чтобы ознакомиться с характеристиками и составными частями шприц-ручки.
Перед началом использования шприц-ручки необходимо исследовать ее на наличие видимых механических повреждений и подтеков (свидетельствующих о нарушении герметичности картриджа). Если Вы не уверены, что шприц-ручка исправна и что у нее нет повреждений, не используйте ее. Проверяйте шприц-ручку перед каждой инъекцией.
Тщательно следуйте инструкции по использованию шприц-ручки: предотвращайте ее падение и влияние на нее прочих внешних факторов (температурное воздействие, прямые солнечные лучи, механическое повреждение и пр.). Если шприц-ручка повреждена, Вы должны утилизировать ее и начать использовать новую.
Если Вы не можете различить цифры на счетчике дозы, Вы должны использовать шприц-ручку под контролем медицинского персонала или других людей с хорошим зрением, прошедших обучение по введению препарата предварительно заполненной шприц-ручкой.
Лица, осуществляющие уход за пациентом, должны обращаться с использованными иглами с особой осторожностью, чтобы предотвратить случайный укол и перекрестное инфицирование.
Предварительно заполненная шприц-ручка с препаратом Семвелика® и игла

I. Подготовка шприц-ручки с новой иглой к использованию
Проверьте название на этикетке шприц-ручки. Необходимо убедиться, что внутри содержится препарат Семвелика® (0.25, 0.5 или 1 мг/доза). Это особенно важно, если Вы применяете более одного инъекционного препарата.
Удерживая шприц-ручку одной рукой, другой снимите колпачок со шприц-ручки, потянув за него.


Убедитесь, что раствор в шприц-ручке бесцветный или почти бесцветный и прозрачный. Посмотрите в окошко держателя картриджа шприц-ручки.
Примечание: если раствор мутный, не бесцветный или есть посторонние примеси, такую шприц-ручку использовать нельзя. Возьмите новую иглу и удалите защитную наклейку.
Примечание: используйте иглы строго в соответствии с рекомендациями врача. Для каждой инъекции используйте новую иглу, чтобы свести к минимуму риск введения неправильной дозы препарата, инфицирования и травмирования тканей.


При помощи наружного колпачка иглы установите ее точно на держатель картриджа. Надежно прикрутите иглу, чтобы она плотно держалась на шприц-ручке.
Снимите наружный колпачок иглы, но не выбрасывайте его. Он понадобится после завершения инъекции, чтобы безопасно снять иглу со шприц-ручки.


Снимите и выбросите внутренний колпачок иглы. Удерживайте шприц-ручку иглой вверх.
Примечание: игла становится видимой по мере удаления внутреннего колпачка.

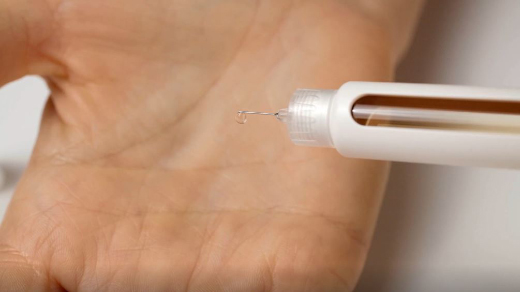
При установке иглы на держатель картриджа на конце иглы может появиться капля препарата - это нормальное явление, однако, если шприц-ручка используется в первый раз, все равно необходимо проверить поступление препарата через иглу. Присоединяйте новую иглу к шприц-ручке непосредственно перед инъекцией, когда пациент будет готов к введению препарата.
II. Проверка поступления препарата через иглу
Перед первым применением шприц-ручки необходимо проверить поступление препарата через иглу. Прокрутите селектор дозы до символа проверки поступления препарата таким образом, чтобы символ совпадал с указателем дозы.
Примечание: если селектор дозы проскочил необходимый символ, прокрутите его в противоположном направлении, чтобы скорректировать положение символа проверки.
Если шприц-ручка уже находится в использовании, начинайте использование с этапа III "Установка дозы".
Держа шприц-ручку иглой вверх, нажимайте и удерживайте пусковую кнопку в этом положении, селектор дозы издаст щелчок, в дозировочном окне появится значение "0". На конце иглы должна появиться капля препарата.


Если после проверки поступления препарата капля не появилась на конце иглы, необходимо повторить действия этапа II "Проверка поступления препарата через иглу", но не более 6 раз. Если капля препарата так и не появилась, необходимо заменить иглу и повторить действия этапа II еще раз. Если капля раствора так и не появилась, необходимо утилизировать шприц-ручку и использовать новую.
Перед использованием шприц-ручки в первый раз следует убедиться в том, что игла хорошо пропускает препарат, а на конце иглы появилась капля раствора. Это гарантирует введение препарата. Если игла повреждена или закупорена, капля раствора не появится и препарат не будет введен, даже если селектор дозы и счетчик дозы будут двигаться. Пациент не сможет ввести необходимую дозу, и эффект препарата Семвелика® не будет достигнут. Необходимо обязательно проверять поступление препарата через иглу перед первой инъекцией.
III. Установка дозы
Перед каждой инъекцией необходимо проверять, какую дозу препарата (мг) пациент набрал по счетчику дозы и указателю дозы. Не ориентируйтесь на щелчки шприц-ручки, не следует их считать.
На шприц-ручке можно выбирать дозы 0.25, 0.5 или 1 мг. Выбор осуществляется селектором дозы. При правильном наборе дозы счетчик дозы и указатель дозы покажут количество мг препарата, соответствующее выбранной пациентом дозировке.
Пациент может выбрать до 1 мг препарата на дозу. Если в шприц-ручке содержится менее 1 мг, счетчик дозы остановится прежде, чем появится значение "1.0".
Поворачивайте селектор дозы до тех пор, пока он не покажет необходимую дозировку - 0.25, 0.5 или 1 мг. Выбранная дозировка должна находиться точно напротив указателя дозы.
Примечание: если дозировка была выбрана неверно, поворотным движением селектора дозы вперед или назад установите правильную.
Для определения остаточного количества препарата необходимо использовать счетчик дозы, поворачивая селектор дозы до остановки счетчика. Если в дозировочном окне он показывает значение "1.0", в шприц-ручке осталось не менее 1 мг препарата. Если счетчик дозы остановился до значения "1.0", это означает, что в шприц-ручке осталось недостаточное количество препарата, чтобы ввести полную дозу 1 мг.

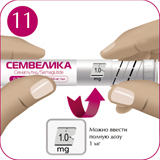
Важно! Не используйте шприц-ручку, если препарата недостаточно для введения полной дозы. Используйте новую шприц-ручку.
IV. Введение препарата
Одним движением руки введите иглу под кожу.
Примечание: используйте техники инъекций, рекомендованные врачом или медсестрой.
Убедитесь, что дозировочное окно находится в поле зрения человека, проводящего инъекцию. Нажмите на пусковую кнопку и удерживайте ее, пока значение "0" не совпадет с указателем дозы. При нажатии на кнопку пациент может услышать или ощутить щелчок. Нельзя дотрагиваться пальцами до счетчика дозы в дозировочном окне - это может прервать инъекцию.

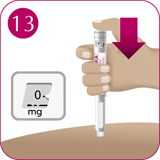
Удерживайте иглу под кожей после того, как счетчик дозы вернется к значению "0", и медленно считайте от одного до десяти.
Примечание: если извлечь иглу из-под кожи раньше, пациент может увидеть, как препарат вытекает из иглы. Это будет означать, что введена неполная доза препарата.
Осторожно извлеките иглу из-под кожи.
Примечание: если в месте инъекции появилась кровь, необходимо слегка прижать к месту укола ватный тампон. Не следует массировать место укола. После завершения инъекции пациент может увидеть каплю раствора на конце иглы. Это нормально и не влияет на введенную дозу препарата.

V. Утилизация иглы
Важно! После каждой инъекции препарата всегда удаляйте иглу из шприц-ручки. Это может предотвратить закупорку игл, загрязнение, инфицирование, вытекание раствора и введение неверной дозы препарата.
Хранить и транспортировать шприц-ручку необходимо без иглы!
После завершения инъекции осторожно и плотно закройте наружным колпачком иглу.
Открутите иглу и выбросите ее вместе с внешней насадкой, соблюдая меры предосторожности.
Примечание: при утилизации использованных игл соблюдайте требования, нормы и правила обращения с потенциально инфицированными материалами.


Закройте колпачком шприц-ручку и храните ее до следующего использования, согласно условиям хранения, указанным в инструкции по применению препарата.

VI. Уход за шприц- ручкой
Со шприц-ручкой следует обращаться аккуратно. Небрежное или неправильное обращение может стать причиной ошибки в дозировании препарата Семвелика®.
Необходимо предохранять шприц-ручку от попадания пыли, грязи и жидкостей.
Запрещается мыть шприц- ручку. По мере загрязнения ее можно протирать влажной тканью, смоченной мягким моющим средством.
Если шприц-ручка подверглась физическому воздействию (удар, вибрация, температурные воздействия и т.п.) или пациент сомневается в ее исправности, необходимо присоединить новую иглу и проверить поступление препарата перед тем, как сделать инъекцию.
Запрещается оставлять шприц-ручку в местах, где она может подвергаться воздействию слишком высоких или слишком низких температур (в автомобиле, на подоконнике и т.д.).
Запрещается проводить инъекцию препаратом Семвелика®, если он был заморожен.
Использованную (пустую) шприц-ручку необходимо выбросить. Выбрасывать пустую шприц-ручку с отсоединенной иглой необходимо в соответствии с рекомендациями, данными врачом, медсестрой, фармацевтом, или с требованиями по утилизации отходов, распространяющими на территории РФ.
Побочное действие
Наиболее часто регистрируемыми нежелательными реакциями (HP) во время КИ являлись нарушения со стороны ЖКТ, включая тошноту (очень часто), диарею (очень часто) и рвоту (часто). В целом данные реакции были легкой или средней степени тяжести и краткосрочными.
HP распределены по системно-органным классам в соответствии с MedDRA с указанием частоты их возникновения согласно рекомендациям ВОЗ:
очень часто (≥1/10), часто (от ≥1/100 до <1/10), нечасто (от ≥1/1000 до <1/100), редко (от ≥1/10000 до <1/1000), очень редко (<1/10000), частота неизвестна (на основании имеющихся данных оценить невозможно).
В каждой группе частоты развития HP представлены по снижению степени серьезности.
Таблица 2. Частота HP при применении семаглутида
| Очень часто | Часто | Нечасто | Редко | Частота неизвестна |
| Со стороны иммунной системы | ||||
| Гиперчувствительностьa | Анафилактические реакции | |||
| Со стороны обмена веществ и питания | ||||
| Гипогликемияb при совместном применении с инсулином или производным сульфонилмочевины | Гипогликемияb при совместном применении с другими ПГГП | |||
| Снижение аппетита | ||||
| Со стороны нервной системы | ||||
| Головокружение | Дисгевзия | |||
| Со стороны органа зрения | ||||
| Осложнения диабетической ретинопатииc | ||||
| Со стороны сердца | ||||
| Увеличение частоты сердечных сокращений | ||||
| Со стороны ЖКТ | ||||
| Тошнота | Рвота | Острый панкреатит | Кишечная непроходимостьd | |
| Диарея | Боль в животе | |||
| Вздутие живота | ||||
| Запор | ||||
| Диспепсия | ||||
| Гастрит | ||||
| Гастроэзофагеальная рефлюксная болезнь | ||||
| Отрыжка | ||||
| Метеоризм | ||||
| Со стороны печени и желчевыводящих путей | ||||
| Холелитиаз | Холангит Холестатическая желтуха | |||
| Со стороны кожи и подкожных тканей | ||||
| Ангионевротический отекd | ||||
| Общие нарушения и реакции в месте введения | ||||
| Утомляемость | Реакции в месте введения | |||
| Лабораторные и инструментальные данные | ||||
| Повышение активности липазы | ||||
| Повышение активности амилазы | ||||
| Снижение массы тела | ||||
а Групповой термин, включающий также НР, связанные с гиперчувствительностью, такие как сыпь и крапивница.
b Гипогликемия, определенная как тяжелая (требующая помощи другого человека) или симптоматическая в сочетании с концентрацией глюкозы в плазме крови <3.1 ммоль/л.
с Осложнения диабетической ретинопатии - это одновременно необходимость в фотокоагуляции сетчатки глаза, необходимость в интравитреальном введении препаратов, кровоизлияние в стекловидное тело, развитие слепоты, связанной с СД. Частота основана на исследовании СС исходов.
d НР из постмаркетинговых исследований.
Двухлетнее исследование сердечно-сосудистых исходов и безопасности
В популяции пациентов с высоким риском развития сердечно-сосудистых заболеваний профиль HP был аналогичным таковому в других КИ фазы 3а (см. подраздел "Клиническая эффективность и безопасность").
Описание отдельных НР
Гипогликемия
Во время монотерапии семаглутидом не наблюдалось эпизодов тяжелой гипогликемии. Гипогликемия тяжелой степени наблюдалась в основном при применении семаглутида в комбинации с производным сульфонилмочевины или инсулином.
Было несколько эпизодов тяжелой гипогликемии при применении семаглутида в комбинации с другими препаратами, за исключением производного сульфонилмочевины, ПГГП.
Гипогликемия по классификации Американской диабетической ассоциации наблюдалась у 11.3% (0.3 случая/пациента в год) пациентов при добавлении семаглутида в дозе 1 мг к терапии ингибитором SGLT2 по сравнению с 2% (0.04 случая/пациента в год) пациентов, получавших плацебо. О тяжелой гипогликемии сообщалось у 0.7% (0.01 случая/пациента в год) и 0% пациентов, соответственно.
HP со стороны ЖКТ
Во время терапии семаглутидом в дозах 0.5 мг и 1 мг у пациентов отмечалась тошнота, диарея и рвота. Большинство реакций были от легкой до средней степени тяжести и краткосрочными. HP стали причиной преждевременного выбывания из КИ 3.9% и 5.9% пациентов, соответственно. Чаще всего о HP сообщалось в первые месяцы терапии.
У пациентов с низкой массой тела при лечении семаглутидом может возникать больше HP со стороны ЖКТ.
В КИ при одновременном применении ингибитора SGLT2 и семаглутида запор и гастроэзофагеальная рефлюксная болезнь наблюдались у 6.7% и 4% пациентов, получавших семаглутид в дозе 1 мг, и пациентов, получавших только ингибитор SGLT2, соответственно. Распространенность этих событий со временем не уменьшалась.
Острый панкреатит
Частота развития острого панкреатита, подтвержденного по результатам экспертной оценки, в исследованиях фазы 3a составила 0.3% при применении семаглутида и 0.2% при применении препарата сравнения. В 2-летнем исследовании сердечно-сосудистых исходов частота развития острого панкреатита, подтвержденная по результатам экспертной оценки, составила 0.5% при применении семаглутида и 0.6% при применении плацебо (см. раздел "Особые указания").
Осложнения диабетической ретинопатии
В двухлетнем КИ с участием пациентов с СД2 и высоким сердечно-сосудистым риском, длительным течением СД и неадекватным контролем гликемии подтвержденные случаи осложнений диабетической ретинопатии развивались у большего количества пациентов, получавших семаглутид (3%), по сравнению с пациентами, получавшими плацебо (1.8 %). У пациентов с анамнезом диабетической ретинопатии в начале КИ возрастание абсолютного риска развития осложнений было выше. У пациентов с отсутствием подтвержденного анамнеза диабетической ретинопатии количество событий было одинаковым при применении семаглутида и плацебо.
В КИ продолжительностью до 1 года частота HP, связанных с диабетической ретинопатией, была одинаковой в группе семаглутида и препаратов сравнения.
Прекращение лечения по причине HP
Частота прекращения лечения по причине HP составила 6.1% и 8.7% для пациентов, получавших семаглутид в дозах 0.5 мг и 1 мг соответственно, по сравнению с 1.5% для пациентов, получавших плацебо. Наиболее часто к прекращению лечения приводили нарушения со стороны ЖКТ.
Реакции в месте введения
Сообщалось о реакциях в месте введения (таких как сыпь в месте введения, покраснение) у 0.6% и 0.5% пациентов, получавших семаглутид в дозах 0.5 мг и 1 мг соответственно. Эти реакции, как правило, носили легкий характер.
Иммуногенность
Вследствие потенциальных иммуногенных свойств белковых и пептидных лекарственных препаратов у пациентов могут появиться антитела к семаглутиду после терапии семаглутидом. В конце КИ доля пациентов, у которых были обнаружены антитела к семаглутиду в любой момент времени, была низкой (1-3%), и ни у одного пациента не было обнаружено нейтрализующих антител к семаглутиду или антител с эффектом, нейтрализующим эндогенный ГПП-1.
Увеличение частоты сердечных сокращений
На фоне применения агонистов рецепторов ГПП-1 отмечалось увеличение ЧСС. У пациентов, получавших семаглутид в исследованиях фазы 3а, наблюдалось среднее увеличение ЧСС на 1-6 уд/мин по сравнению с исходным уровнем 72-76 уд/мин. В долгосрочном исследовании с участием пациентов с СС факторами риска 16% пациентов, получавших лечение семаглутидом, имели увеличение ЧСС на 10 уд/мин по сравнению с 11% пациентов, получавших плацебо, после 2 лет лечения.
Противопоказания к применению
- повышенная чувствительность к семаглутиду или любому из вспомогательных веществ, входящих в состав препарата;
- медуллярный рак щитовидной железы в анамнезе, в т.ч. в семейном;
- множественная эндокринная неоплазия (МЭН) 2 типа;
- сахарный диабет 1 типа (СД1);
- диабетический кетоацидоз.
Противопоказано применение препарата Семвелика® у следующих групп пациентов и при следующих состояниях/заболеваниях в связи с отсутствием данных по эффективности и безопасности или ограниченным опытом применения:
- беременность;
- период грудного вскармливания;
- возраст до 18 лет;
- печеночная недостаточность тяжелой степени;
- терминальная стадия почечной недостаточности (КК <15 мл/мин);
- хроническая сердечная недостаточность (ХСН) IV функционального класса (в соответствии с классификацией NYHA (Нью-Йоркская кардиологическая ассоциация)).
С осторожностью у пациентов с почечной недостаточностью и у пациентов с наличием панкреатита в анамнезе (см. раздел "Особые указания").
Применение при беременности и кормлении грудью
Беременность
Исследования на животных продемонстрировали репродуктивную токсичность препарата (см. раздел "Доклинические данные по безопасности").
Данные по применению семаглутида у беременных женщин ограничены. Противопоказано применять семаглутид во время беременности.
Женщинам с сохраненным репродуктивным потенциалом рекомендуется использовать контрацепцию во время терапии семаглутидом.
Если пациентка готовится к беременности, либо беременность уже наступила, терапию семаглутидом необходимо прекратить. Из-за длительного периода полувыведения терапию семаглутидом необходимо прекратить как минимум за 2 месяца до планируемого наступления беременности (см. раздел "Фармакокинетика").
Период грудного вскармливания
У лактирующих крыс семаглутид проникал в молоко. Нельзя исключить риск для ребенка, находящегося на грудном вскармливании. Противопоказано применять семаглутид в период грудного вскармливания.
Фертильность
Действие семаглутида на фертильность у людей неизвестно. Семаглутид не влиял на фертильность самцов крыс. Среди самок крыс увеличение эстрального цикла и незначительное снижение количества овуляций наблюдалось при дозах, вызывавших снижение массы тела самки.
Применение при нарушениях функции печени
Применение при нарушениях функции почек
Применение у детей
Применение у пожилых пациентов
Особые указания
Применение семаглутида противопоказано у пациентов с СД1 или для лечения диабетического кетоацидоза.
Семаглутид не заменяет инсулин. Диабетический кетоацидоз был зарегистрирован у инсулинозависимых пациентов, у которых отмечалось быстрое прекращение лечения или снижение дозы инсулина при начале лечения агонистом ГПП-1Р (см. раздел "Способ применения и дозы").
Риск развития аспирации при проведении оперативных вмешательств под общей анестезией или глубокой седацией
Сообщалось о случаях аспирационной пневмонии у пациентов, получавших агонисты рецепторов ГПП-1 при проведении оперативных вмешательств под общей анестезией или глубокой седацией. Таким образом, следует учитывать повышенный риск присутствия остаточного желудочного содержимого из-за задержки опорожнения желудка перед выполнением процедуры под общим наркозом или глубокой седацией.
Реакции со стороны ЖКТ
Применение агонистов ГПП-1Р может быть ассоциировано с HP со стороны ЖКТ. Это следует учитывать при лечении пациентов с почечной недостаточностью, т.к. тошнота, рвота и диарея могут привести к дегидратации и ухудшению функции почек.
Острый панкреатит
При применении агонистов ГПП-1Р наблюдались случаи развития острого панкреатита. Пациенты должны быть проинформированы о характерных симптомах острого панкреатита. При подозрении на панкреатит терапия семаглутидом должна быть прекращена; в случае подтверждения острого панкреатита терапию препаратом Семвелика® возобновлять не следует. Следует соблюдать осторожность у пациентов с панкреатитом в анамнезе.
При отсутствии других признаков и симптомов острого панкреатита повышение активности ферментов поджелудочной железы не является прогностическим фактором развития острого панкреатита.
Реакции со стороны печени и желчевыводящих путей
При применении агонистов ГПП-1Р возможно развитие желчекаменной болезни, холецистита, холангита и холестатической желтухи. При появлении абдоминальных симптомов, таких как боли в животе, следует принять соответствующие меры, например, при необходимости провести детальное обследование с целью выяснения причины с помощью визуализирующих диагностических методов и т.д.
Гипогликемия
Пациенты, получающие семаглутид в комбинации с производным сульфонилмочевины или инсулином, могут иметь повышенный риск развития гипогликемии. В начале лечения препаратом Семвелика® риск развития гипогликемии можно снизить, уменьшив дозу производного сульфонилмочевины или инсулина.
Диабетическая ретинопатия
Наблюдалось повышение риска развития осложнений диабетической ретинопатии у пациентов с наличием диабетической ретинопатии, получающих терапию инсулином и семаглутидом (см. раздел "Побочное действие"). Следует соблюдать осторожность при применении семаглутида у пациентов с диабетической ретинопатией, получающих инсулинотерапию. Такие пациенты должны находиться под постоянным наблюдением и получать лечение в соответствии с клиническими рекомендациями. Быстрое улучшение гликемического контроля было ассоциировано с временным ухудшением состояния диабетической ретинопатии, однако при этом нельзя исключать и другие причины.
Сердечная недостаточность
Отсутствует опыт применения семаглутида у пациентов с ХСН IV функционального класса в соответствии с классификацией NYHA. Применение препарата у таких пациентов противопоказано.
Заболевания щитовидной железы
В пострегистрационном периоде применения другого аналога ГПП-1, лираглутида, были отмечены случаи медуллярного рака щитовидной железы (МРЩЖ). Имеющихся данных недостаточно для установления или исключения причинно-следственной связи возникновения МРЩЖ с применением аналогов ГПП-1. Необходимо проинформировать пациента о риске МРЩЖ и о симптомах опухоли щитовидной железы (появления уплотнения в области шеи, дисфагии, одышки, непроходящей охриплости голоса).
Значительное повышение концентрации кальцитонина в плазме крови может указывать на МРЩЖ (у пациентов с МРЩЖ значения концентрации кальцитонина в плазме крови обычно >50 нг/л). При выявлении повышения концентрации кальцитонина в плазме крови следует провести дальнейшее обследование пациента. Пациенты с узлами в щитовидной железе, выявленными при медицинском осмотре или при проведении УЗИ щитовидной железы, также должны быть дополнительно обследованы.
Применение семаглутида у пациентов с личным или семейным анамнезом МРЩЖ или с синдромом МЭН типа 2 противопоказано.
Фертильность
Действие семаглутида на фертильность у людей неизвестно. Семаглутид не влиял на фертильность самцов крыс. Среди самок крыс увеличение эстрального цикла и незначительное снижение количества овуляций наблюдалось при дозах, вызывавших снижение массы тела самки.
Влияние на способность к управлению транспортными средствами и механизмами
Семаглутид не влияет или незначительно влияет на способность управлять транспортными средствами или работу с механизмами. Пациенты должны быть предупреждены о том, что им следует соблюдать меры предосторожности во избежание развития у них гипогликемии во время управления транспортными средствами и при работе с механизмами, особенно при применении семаглутида в комбинации с производным сульфонилмочевины или инсулином.
Передозировка
Симптомы: в ходе КИ сообщалось о передозировках до 4 мг в однократной дозе и до 4 мг в неделю. Наиболее частой HP, о которой сообщалось, была тошнота. Все пациенты выздоровели без осложнений.
Лечение: специфического антидота при передозировке семаглутидом не существует. Рекомендуется проведение соответствующей симптоматической терапии. Учитывая длительный период выведения препарата (примерно 1 неделя), может потребоваться продолжительный период наблюдения и лечения симптомов передозировки.
Лекарственное взаимодействие
Исследования семаглутида in vitro показали очень небольшую вероятность ингибирования или индукции изоферментов системы цитохрома Р450 (CYP) и ингибирования транспортеров лекарственных препаратов.
Задержка опорожнения желудка при применении семаглутида может оказывать влияние на всасывание сопутствующих пероральных лекарственных препаратов. Семаглутид следует применять с осторожностью у пациентов, получающих пероральные лекарственные препараты, для которых необходима быстрая абсорбция в ЖКТ.
Парацетамол
При оценке фармакокинетики парацетамола во время теста стандартизированного приема пищи было выявлено, что семаглутид задерживает опорожнение желудка. При одновременном применении семаглутида в дозе 1 мг AUC0-60 и Сmax парацетамола снизились на 27% и 23% соответственно. Общая экспозиция парацетамола (AUC0-5) при этом не изменялась. При одновременном приеме семаглутида и парацетамола коррекция дозы последнего не требуется.
Пероральные гормональные контрацептивные средства
Не предполагается, что семаглутид снижает эффективность пероральных гормональных контрацептивных средств. При одновременном применении комбинированного перорального гормонального контрацептивного препарата (0.03 мг этинилэстрадиола/0.15 мг левоноргестрела) и семаглутида последний не оказывал клинически значимого влияния на общую экспозицию этинилэстрадиола и левоноргестрела. Экспозиция этинилэстрадиола не была затронута; наблюдалось увеличение экспозиции левоноргестрела в равновесном состоянии на 20%. Сmax не изменилась ни для одного из компонентов.
Аторвастатин
Семаглутид не изменял системную экспозицию аторвастатина после применения однократной дозы аторвастатина (40 мг). Сmax аторвастатина снизилась на 38%. Это изменение было расценено как клинически незначимое.
Дигоксин
Семаглутид не изменял системную экспозицию или Сmax дигоксина после применения однократной дозы дигоксина (0.5 мг).
Метформин
Семаглутид не изменял системную экспозицию или Сmax метформина после применения метформина в дозе 500 мг 2 раза/сут в течение 3.5 суток.
Варфарин
Семаглутид не изменял системную экспозицию или Сmax R- и S-изомеров варфарина после применения однократной дозы варфарина (25 мг). На основании определения МНО клинически значимых изменений фармакодинамических эффектов варфарина также не наблюдалось.
Несовместимость
Другие вещества, добавленные к семаглутиду, могут вызвать разрушение семаглутида. Семаглутид нельзя смешивать с другими лекарственными средствами, в т.ч. с инфузионными растворами.
Условия хранения препарата Семвелика®
Препарат следует хранить в защищенном от света, недоступном для детей месте, при температуре от 2°С до 8°С (в холодильнике), но не рядом с морозильной камерой. Не замораживать.
Срок годности препарата Семвелика®
Используемую или переносимую в качестве запасной шприц-ручку с препаратом хранить при температуре не выше 30°С или при температуре от 2°С до 8°С (в холодильнике) в течение 6 недель. Не замораживать. После использования закрывать шприц-ручку колпачком для защиты от света.
Препарат Семвелика® следует предохранять от воздействия избыточного тепла и света.
Условия реализации
Контакты для обращений
ИЗВАРИНО ФАРМА ООО (Россия)

|
|
108817 Москва, п. Внуковское, |
X